- 标准下载 加入收藏
-
183 5749 2502
199 5745 8308

质量管理体系
您的位置:首页 > 服务项目 > 质量管理体系国内:第二类、第三类医疗器械生产企业应当向所在地省、自治区、直辖市药品监督管理部门申请生产许可。
欧盟:需要公告机构介入的CE认证需要符合ISO 13485要求,通过公告机构认证。
美国:通过FDA认证,体系需要符合QSR 820。
医疗器械企业应当按照规范的要求,结合产品特点,建立健全与所生产医疗器械相适应的质量管理体系,并保证其有效运行。
医疗器械质量管理体系具有很强的专业性,其中涉及到机构与人员、厂房与设施、设备、文件管理、设计开发、采购、生产管理、质量控制、销售和售后服务、不合格品控制、不良事件监测、分析和改进等方方面面。
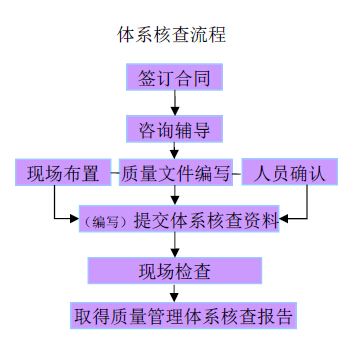
我们的服务:
体系管理咨询;
ISO 13485辅导咨询;
QSR 820辅导咨询;
飞行检查质量体系合规整改服务;
年度顾问服务。

电话

微信
 微信联系
微信联系 公众号
公众号
咨询
 1458335814
1458335814 546452726
546452726
邮箱